2026年3月30日,先聲藥業(2096.HK)宣布,與康乃德生物醫藥合作的創新抗體藥物樂德奇拜單抗針對成人、青少年中重度特應性皮炎患者的Ⅲ期臨床研究入選第84屆美國皮膚科學會年會最新突破性研究摘要(Late-Breaking Abstract, LBA)并進行口頭報告。
研究數據顯示,樂德奇拜單抗2周即可快速緩解瘙癢、改善皮膚炎癥,且深度清除皮損的療效可維持至52周。該研究由北京大學人民醫院張建中教授和周城教授聯合牽頭擔任主要研究者。3月28日,周城教授代表研究團隊在美國科羅拉多州丹佛市的會議現場向國際學術界進行了報告。
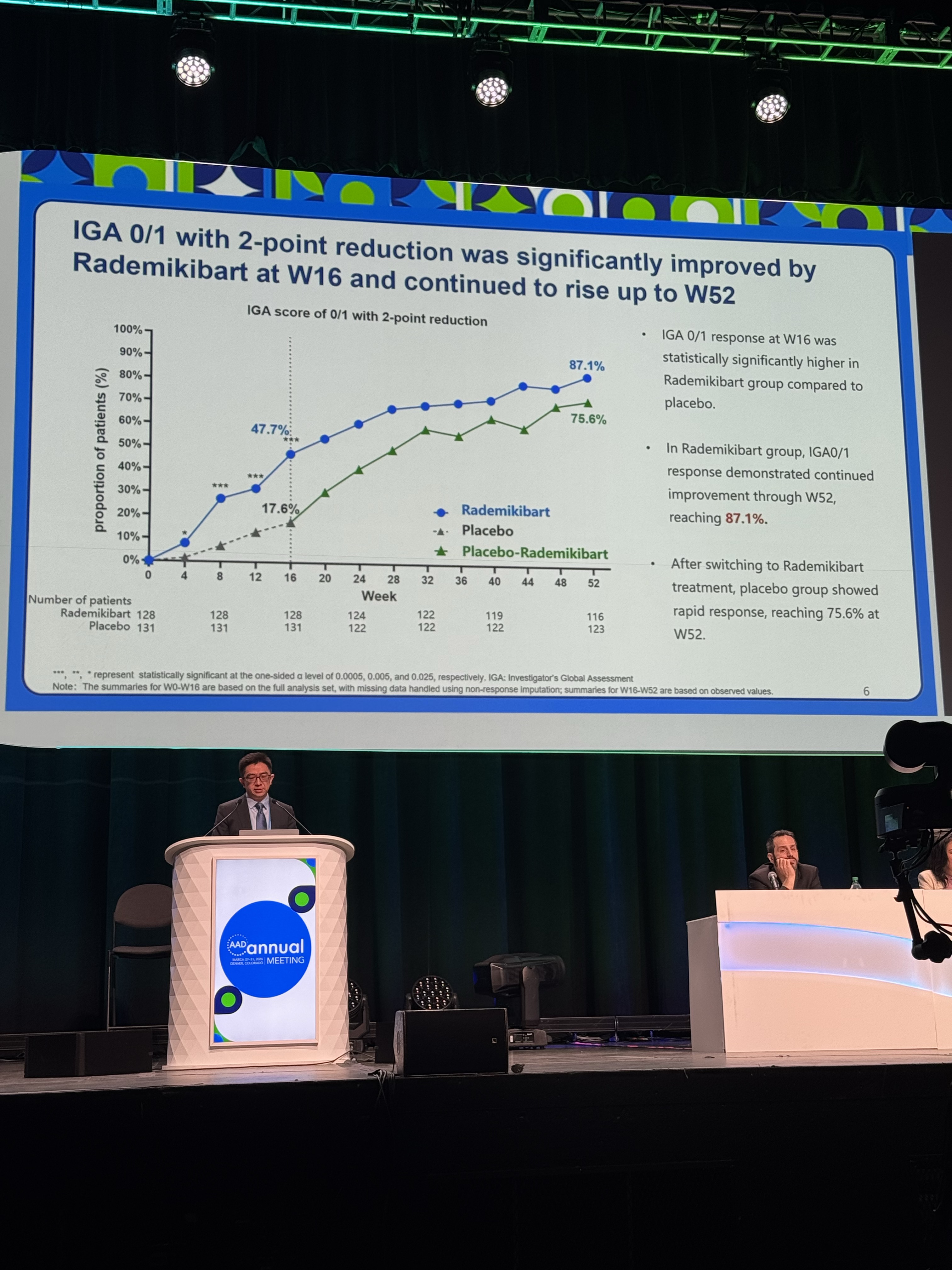
圖:周城教授在AAD年會現場做口頭報告
特應性皮炎(AD)以反復發作的慢性濕疹樣皮疹為主要表現,伴有顯著的皮膚干燥和瘙癢。據估算,我國現有AD患者約7000萬,且呈增長趨勢。其中,中重度患者占比接近50%。AD因患者群體龐大,且顯著影響患者生活質量,被稱為皮膚科的“一號疾病”。盡管已有生物制劑上市,但臨床仍面臨深度緩解率不足,易復發等挑戰,目前的治療選擇仍有限。患者對療效更好且安全性更優的新藥需求迫切。
在本次隨機、雙盲、安慰劑對照的Ⅲ期臨床試驗(RADIANT-AD,NCT06477835)中,共入組259例中重度AD成人和青少年受試者。患者按1:1隨機分配接受樂德奇拜單抗或安慰劑治療16周,隨后進入為期36周的開放標簽期,所有受試者均接受樂德奇拜單抗治療。
療效結果:
第16周時,接受樂德奇拜單抗治療的患者達到以下療效指標的比例均顯著優于安慰劑組(p<0.0001):
1、 研究者總體評估(IGA)達到0或1分且較基線降低≥2分( 47.7% vs.17.6%)
2、 濕疹面積與嚴重程度指數(EASI)改善≥75% (74.2% vs. 34.4%)
3、 濕疹面積與嚴重程度指數(EASI)改善≥90%(43.0% vs. 14.5%)
4、 瘙癢數字評分量表(NRS)降低≥3分(54.7% vs. 27.5%)
第52周時,樂德奇拜單抗的療效持續并進一步顯現,達到上述指標的比例分別為87.1%、96.6%、85.3%、91.2%。
安全性數據:
樂德奇拜單抗在長期治療(0-52周)中具有良好的安全性特征,與其他抗 IL-4 單克隆抗體一致。第16周時,樂德奇拜單抗組與安慰劑組治療期不良事件(TEAE)發生率分別為60.9%與64.9%;第52周時,樂德奇拜單抗組TEAE發生率為82.2%。第16周時,樂德奇拜單抗組的嚴重不良事件和因不良事件導致的永久停藥率較低,至第52周時仍保持較低水平。
張建中教授表示:“樂德奇拜單抗在臨床研究中呈現出‘療效與安全性雙優’的特點,尤其是其長期安全性表現更增強了臨床信心。對臨床而言,樂德奇拜單抗的意義已不只是新增一種治療手段,更在于它有望成為推動中重度AD治療目標持續升級、促進長期規范管理落地的重要力量。”
周城教授表示:“樂德奇拜單抗展現出對AD癥狀持續深度緩解能力,不僅能快速起效,在持續治療后獲益更進一步提升,且安全性良好。這意味著藥物有望針對中重度AD患者長期管理的核心難點,為臨床醫生和患者提供一種安全有效的新選擇。”
樂德奇拜單抗是靶向IL-4Rα的全人源單抗。臨床前研究顯示其與受體的親和力高于度普利尤單抗,可抑制IL-4和IL-13的生物活性,通過阻斷Th2型炎癥通路,發揮對AD、哮喘等炎癥性疾病的治療價值。
2023年11月,先聲藥業與康乃德生物醫藥訂立獨家許可與合作協議,獲得在大中華地區開發、生產和商業化樂德奇拜單抗所有適應癥的獨家權利。此后,先聲藥業與全國59家臨床中心的專家協同合作,迅速啟動了該藥物治療AD的關鍵性Ⅲ期臨床研究,并已達到主要研究終點。此次Ⅲ期臨床數據的公布,為藥物的差異化臨床價值提供了重磅證據。2025年7月,樂德奇拜單抗的新藥上市申請(NDA)已獲國家藥監局受理,有望為中國AD患者帶來更有效治療藥物。
關于先聲藥業
先聲藥業(2096.HK)是一家創新與研發驅動的制藥公司,建設有“神經與腫瘤藥物研發全國重點實驗室”。公司聚焦神經科學、抗腫瘤、自身免疫及抗感染領域,同時積極前瞻性布局未來有重大臨床需求的疾病領域,履行“為患者而生”的企業使命。公司以自主研發及協同創新雙輪驅動,與多家創新企業、科研院校建立戰略合作伙伴關系。更多信息請訪問:www.0371hn.cn
關于康乃德生物醫藥
康乃德生物醫藥是一家擁有臨床階段產品及全球化布局的生物醫藥公司,致力于開發治療慢性炎癥性疾病的創新療法,改善全球數百萬患者的生活。康乃德生物醫藥核心在研產品樂德奇拜單抗是一種IL-4Rα抗體,已在特應性皮炎和哮喘中展現出療效。公司正就其在治療哮喘急性加重和COPD方面開展全球研究,這兩個領域均存在顯著未被滿足的醫療需求。